近日,華東理工大學(xué)藥學(xué)院高峰教授團(tuán)隊(duì)聯(lián)合唐赟教授團(tuán)隊(duì)在非酒精性脂肪性肝炎治療領(lǐng)域取得重要進(jìn)展,相關(guān)成果以“Chemotaxis-guided nanoplatform for non-alcoholic steatohepatitis therapy via macrophage reprogramming, hepatoprotection and gut microbiome modulation”為題發(fā)表在國(guó)際權(quán)威學(xué)術(shù)期刊Biomaterials上。該研究構(gòu)建了一種仿生膜納米遞藥平臺(tái),利用M2巨噬細(xì)胞膜的炎癥趨化性實(shí)現(xiàn)奧貝膽酸的靶向遞送,同時(shí)通過(guò)整合巨噬細(xì)胞重編程、肝保護(hù)及腸道微生態(tài)調(diào)控等多重機(jī)制,為多元協(xié)同治療非酒精性脂肪性肝炎(Nonalcoholic steatohepatitis,NASH)提供了新策略。
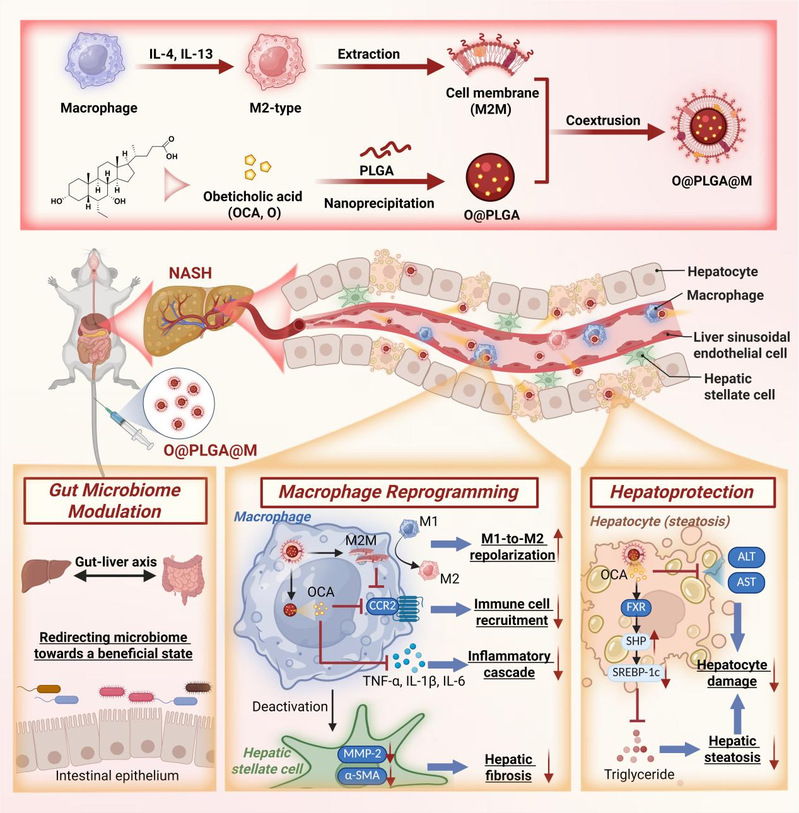
圖片說(shuō)明:O@PLGA@M 靶向遞送奧貝膽酸并調(diào)控肝臟微環(huán)境治療非酒精性脂肪性肝炎的示意圖
NASH的發(fā)病率和死亡逐年攀升,其病理學(xué)特征主要表現(xiàn)為肝臟脂質(zhì)蓄積、炎性反應(yīng)、以及漸進(jìn)性纖維化。奧貝膽酸(Obeticholic acid,OCA)是一種法尼醇X受體(Farnesoid X receptor,F(xiàn)XR)激動(dòng)劑,已被證明可改善NASH癥狀。然而,OCA水溶性差極大限制了其療效,且因缺乏特異靶向性,易引起瘙癢、高密度脂蛋白降低等不良反應(yīng)。
為解決這一問(wèn)題,該研究首次構(gòu)建了M2巨噬細(xì)胞膜仿生納米遞藥平臺(tái)(O@PLGA@M),利用其對(duì)炎癥部位的趨化性,將奧貝膽酸靶向遞送至肝炎病灶。同時(shí),M2巨噬細(xì)胞膜可將促炎的M1巨噬細(xì)胞重編程為抗炎的M2表型,與奧貝膽酸協(xié)同發(fā)揮調(diào)節(jié)脂質(zhì)代謝、抗炎、抗纖維化及肝保護(hù)作用,重塑肝臟微環(huán)境。此外,O@PLGA@M還能通過(guò)腸肝軸調(diào)節(jié)腸道微生物群,進(jìn)一步緩解NASH病理癥狀。該研究對(duì)推動(dòng)奧貝膽酸的臨床轉(zhuǎn)化以及NASH肝臟微環(huán)境調(diào)控具有重要意義。
藥學(xué)院博士研究生潘細(xì)兒和碩士研究生陳心儀為該論文共同第一作者,高峰教授和唐赟教授為通訊作者。上述研究工作得到了上海市細(xì)胞代謝光遺傳學(xué)技術(shù)前沿科學(xué)研究基地、國(guó)家重點(diǎn)研發(fā)計(jì)劃、國(guó)家自然科學(xué)基金及中央高校基本科研業(yè)務(wù)費(fèi)等項(xiàng)目的資助。
原文鏈接:https://doi.org/10.1016/j.biomaterials.2025.123694